Nuevo enfoque para corregir insuficiencias de expresión génica
Publicado originalmente por Olivia Dimmer, Northwestern University, el 17 de noviembre de 2023
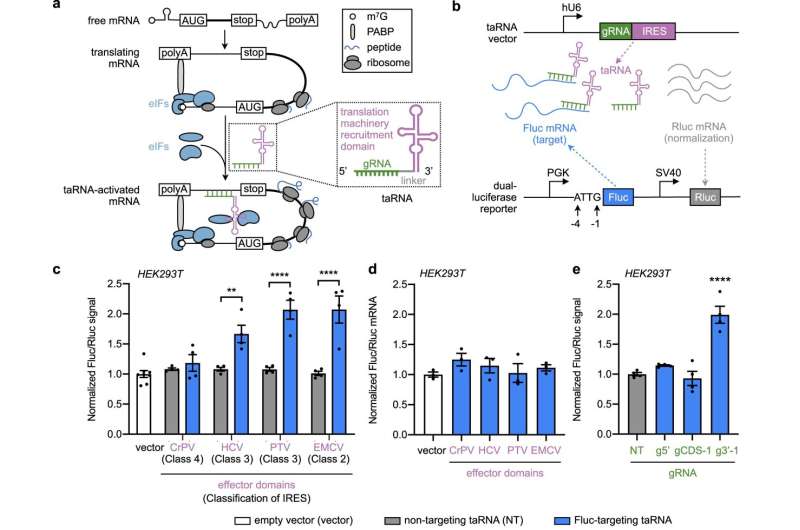
Los taARNs construidos a partir de un conjunto de IRESs aumentan la traducción de genes informativos. Crédito: Nature Communications (2023). DOI: 10.1038/s41467-023-42252-z
Una nueva tecnología molecular, capaz de unirse al ARNm y regular la expresión génica, podría ofrecer una nueva vía para tratar enfermedades causadas por haploinsuficiencia, o ausencia de una copia funcional del gen, según un estudio publicado en Nature Communications.
El ARN mensajero, o ARNm, contiene instrucciones para que el ADN produzca proteínas. Muchas enfermedades, entre ellas el cáncer y muchos otros trastornos genéticos, se deben a una expresión insuficiente de los genes -y, por tanto, de las proteínas-, pero existen pocas estrategias para corregir ese tipo de irregularidad a nivel molecular.
La nueva tecnología, denominada "ARN activador de la traducción" (taARN), consiste en pequeñas moléculas programadas para unirse a moléculas específicas de ARNm, con el fin de controlar directamente su traducción en proteínas, explica el Dr. Alfred L. George Jr. catedrático y profesor Alfred Newton Richards de Farmacología y coautor del estudio.
"Esta tecnología abre la puerta a una nueva forma de potenciar la expresión de un gen a nivel proteínico. Hay muchas formas de eliminar un gen. Hay muy pocas formas de aumentar la regulación del gen y producir más proteínas a partir de la copia del gen que no está inhabilitada por una mutación", dijo George, que también dirige el Centro de Farmacogenómica.
El estudio fue fruto de la colaboración entre George y el doctor Bryan Dickinson, catedrático de Química de la Universidad de Chicago y autor principal del artículo.
En el estudio, los investigadores combinaron fragmentos de secuencias dentro de moléculas de ARN para crear ARNt que pudieran dirigirse a PTEN, un ARNm conocido por actuar como potente supresor de tumores, y a ABCA7, un ARNm que suele ser deficiente en pacientes con enfermedad de Alzheimer. Tras administrar los taARN a células humanas cultivadas, los investigadores comprobaron que los niveles de ambos ARNm habían aumentado.
A continuación, los investigadores programaron los ARNm para que se unieran a PTEN y CDKN1A, otro gen relacionado con la supresión tumoral, en una muestra humana de cáncer de mama agresivo triple negativo. Según el estudio, tras una inyección de taARN, el crecimiento tumoral se redujo a la mitad.
A continuación, George y sus colaboradores utilizaron los ARNt para estimular la producción de SYNGAP1 en neuronas humanas. SYNGAP1 es un importante regulador de la actividad sináptica, y los niños que nacen con una sola copia funcional de este gen padecen epilepsia y graves trastornos del desarrollo neurológico.
Según el estudio, las neuronas humanas generadas en el laboratorio de George a partir de células madre pluripotentes inducidas, derivadas de pacientes que recibieron los taARN, mostraron una restauración de la proteína SYNGAP1 hasta niveles normales.
Los resultados del estudio ofrecen una nueva y prometedora estrategia para tratar diversas enfermedades derivadas de la insuficiencia de la expresión de genes y proteínas, afirmó George.
"El hecho de que este método funcione en neuronas humanas es muy emocionante", afirmó George. "Hay muchas tecnologías que funcionan en el laboratorio en sistemas artificiales, pero no lo hacen tan bien en células humanas. Las neuronas humanas son especialmente difíciles".
El estudio es un gran ejemplo de colaboración institucional que sin duda impulsará nuevos descubrimientos, dijo George.
"El profesorado de la Northwestern ha invertido mucho esfuerzo en desarrollar líneas celulares de niños con trastornos neurogenéticos y del neurodesarrollo poco frecuentes, como la discapacidad intelectual relacionada con SYNGAP1. Este recurso celular es una mina de oro para probar nuevas estrategias terapéuticas, como la que se presenta en este artículo", dijo George.
"Este estudio es un buen ejemplo de colaboración entre instituciones de Chicago, así como entre un biólogo químico y mi laboratorio, que investiga trastornos humanos con modelos de células madre de la enfermedad".
Más información: Yang Cao et al, RNA-based translation activators for targeted gene upregulation, Nature Communications (2023). DOI: 10.1038/s41467-023-42252-z
Información de la revista: Nature Communication
Proporcionado por: Northwestern University


Comentarios
Publicar un comentario